Четыре новых химических элемента были официально добавлены в периодическую таблицу Менделеева. Таким образом был завершён её седьмой ряд. Новые элементы — 113, 115, 117 и 118 — были синтезированы искусственно в лабораториях России, США и Японии (то есть в природе их не существует). Однако официального признания открытий, сделанного группой независимых экспертов, пришлось ждать до конца 2015 года: Международный союз теоретической и прикладной химии объявил о пополнении 30 декабря 2015 года.
Все "новые" элементы были синтезированы в лабораторных условиях с помощью более лёгких ядер атомов. Это в старые добрые времена можно было выделить кислород путём сжигания оксида ртути - теперь же учёным приходится тратить годы и использовать массивные ускорители частиц, чтобы обнаружить новые элементы. К тому же, нестабильные агломерации протонов и нейтронов (именно такими предстают перед учёными новые элементы) держатся вместе лишь доли секунды прежде, чем распасться на более мелкие, но более устойчивые "осколки".
Теперь команды, получившие и доказавшие существование новых элементов таблицы, имеют право выдвинуть новые названия для этих элементов, а также два буквенных символа для их обозначения.
Элементы могут быть названы в честь одного из своих химических или физических свойств, а также по названию минерала, топонима или учёного. Также название может основываться на мифологических именах.
В настоящее время элементы носят неблагозвучные рабочие названия - унунтрий (Uut), унунпентий (Uup), унунсептий (Uus) и унуноктий (Uuo) — что соответствует латинским названиям цифр в их номере.
Ограничения на существование атомных ядер есть и со стороны сверхтяжелых элементов. Элементы с Z > 92 в естественных условиях не обнаружены. Расчеты по жидкокапельной модели предсказывают исчезновение барьера деления для ядер с Z2/A ≈ 46 (примерно 112 элемент). В проблеме синтеза сверхтяжелых ядер следует выделить два круга вопросов.
- Какими свойствами должны обладать сверхтяжелые ядра? Будут ли существовать магические числа в этой области Z и N. Каковы основные каналы распада и периоды полураспада сверхтяжелых ядер?
- Какие реакции следует использовать для синтеза сверхтяжелых ядер, типы бомбардирующих ядер, ожидаемые величины сечений, ожидаемые энергии возбуждения компаунд-ядра и каналы снятия возбуждения?
Так как образование сверхтяжелых ядер происходит в результате полного слияния
ядра мишени и налетающей частицы необходимо создание теоретических моделей,
описывающих динамику процесса слияния двух сталкивающихся ядер в компаунд-ядро.
Проблема синтеза сверхтяжелых элементов тесно связана с тем фактом, что ядра с
Z,N = 8, 20, 28, 50, 82,
N = 126
(магические числа) обладают повышенной стабильностью по отношению к различным
модам радиоактивного распада. Это явление объясняется в рамках оболочечной
модели − магические числа соответствуют заполненным оболочкам. Естественно
возникает вопрос о существовании следующих магических чисел по
Z
и N. В случае, если они
существуют в области N-Z-диаграммы атомных ядер N > 150,
Z > 101,
должны наблюдаться сверхтяжелые ядра, имеющие повышенные периоды полураспада,
т.е. должен существовать Остров Стабильности. В работе на основе расчетов, выполненных с
использованием потенциала Вудса-Саксона с учетом спин-орбитального
взаимодействия, было показано, что повышение стабильности ядер следует ожидать
для ядра с Z = 114, то есть
следующая заполненная протонная оболочка соответствует Z = 114, заполненная нейтронная
оболочка соответствует числу N ~
184.
Замкнутые оболочки могут существенно увеличить высоту барьера деления и
соответственно увеличить время жизни ядра. Таким образом в этой области ядер (Z = 114,
N ~
184)
следует искать Остров Стабильности. Этот же результат был независимо получен в
работе .
Ядра с Z = 101–109 были открыты до 1986 года и получили названия: 101 - Md (Menelevium), 102 - No (Nobelium), 103
- Lr (Lawrencium), 104 - Rf (Rutherfordium, 106 - Sg (Seaborgium), 107 - Ns (Nielsborium),
108 - Hs (Hassium), 109 - Mt (Meitnerium). Учитывая заслуги исследователей из
Дубны в открытии большого числа изотопов тяжелых элементов (102-105), в 1997
году решением Генеральной Ассамблеи чистой и прикладной химии элементу с Z = 105
было присвоено имя Dubnium (Db). Этот элемент ранее назывался Ha (Hannium).
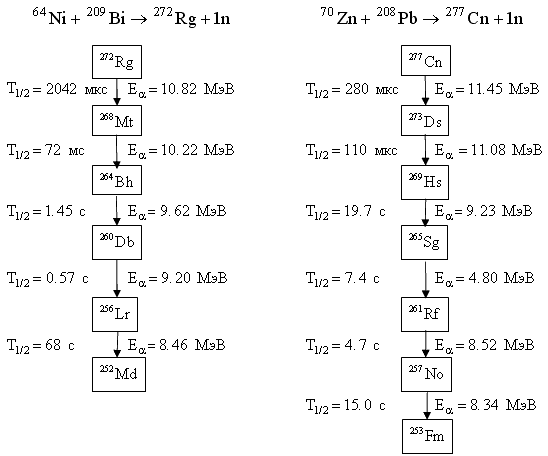
Рис. 12.3. Цепочки распадов изотопов Ds (Z = 110), Rg (Z = 111), Cn (Z = 112).
Новый этап в исследовании сверхтяжелых ядер начался в 1994 году, когда была
существенно повышена эффективность регистрации и усовершенствована методика
наблюдения сверхтяжелых ядер. Как результат были обнаружены изотопы Ds (Z = 110),
Rg
(Z = 111)
и Cn
(Z = 112)
.
Для получения сверхтяжелых ядер использовались ускоренные пучки
50 Ti,
51 V,
58 Fe,
62 Ni,
64 Ni,
70 Zn и
82 Se. В качестве мишеней применялись изотопы
208 Pb и 209
Bi. Различные изотопы 110 элемента были синтезированы в Лаборатории ядерных
реакций им. Г.Н. Флерова с помощью реакции
244 Pu(34 S,5n) 272 110
и в GSI (Дармштадт) в реакции 208 Pb(62 Ni,n) 269 110.
Изотопы 269 Ds,
271 Ds,
272 Rg
и
277 Cn
регистрировались по их цепочкам распада (рис. 12.3).
Большую роль в получении сверхтяжелых элементов играют теоретические модели, с
помощью которых рассчитываются ожидаемые характеристики химических элементов,
реакции, в которых они могут образовываться.
На
основе различных теоретических моделей были рассчитаны распадные характеристики
сверхтяжелых ядер. Результаты одного из таких расчетов показаны на рис. 12.4.
Приведены периоды полураспада четно-четных сверхтяжелых ядер относительно
спонтанного деления (а), α-распада
(б), β-распада
(в) и для всех возможных процессов распада (г). Наиболее устойчивым ядром по
отношению к спонтанному делению (рис. 12.4а) является ядро с Z = 114 и N = 184.
Для него период полураспада по отношению к спонтанному делению ~10 16
лет. Для изотопов 114-го элемента, отличающихся от наиболее устойчивого на 6-8
нейтронов, периоды полураспада уменьшаются на
10-15 порядков. Периоды
полураспада по отношению к α-распаду
приведены на рис. 12.5б. Наиболее устойчивое ядро расположено в области Z = 114
и N = 184 (T 1/2 = 10 15
лет).
Стабильные по отношению к β-распаду
ядра показаны на рис. 12.4в темными точками. На рис. 12.4г приведены полные
периоды полураспада, которые для четно-четных ядер, расположенных внутри
центрального контура, составляют ~10 5
лет. Таким образом, после учета всех типов распада оказывается, что ядра в
окрестности Z = 110 и N = 184 образуют «остров стабильности». Ядро
294 110 имеет период полураспада около 10 9
лет. Отличие величины Z от предсказываемого оболочечной моделью магического
числа 114 связано с конкуренцией между делением (относительно которого ядро с Z = 114
наиболее стабильно) и α-распадом
(относительно которого устойчивы ядра с меньшими Z). У нечетно-четных и
четно-нечетных ядер периоды полураспада по отношению к
α-распаду
и спонтанному делению увеличиваются, а по отношению к β-распаду
уменьшаются. Следует отметить, что приведенные оценки сильно зависят от
параметров, использованных в расчетах, и могут рассматриваться лишь как указания
на возможность существования сверхтяжелых ядер, имеющих времена жизни достаточно
большие для их экспериментального обнаружения.

Рис. 12.4. Периоды полураспада, вычисленные для четно-четных сверхтяжелых ядер
(числа обозначают периоды полураспада в годах):
а − относительно спонтанного деления, б − α-распада,
в − е-захвата и β-распада, г − для всех процессов распада
Результаты еще одного расчета равновесной формы сверхтяжелых ядер и их периодов полураспада показаны на рис. 12.5, 12.6 . На рис. 12.5 показана зависимость энергии равновесной деформации от количества нейтронов и протонов для ядер с Z = 104-120. Энергия деформации определяется как разность энергий ядер в равновесной и сферической форме. Из этих данных видно, что в области Z = 114 и N = 184 должны располагаться ядра, имеющие в основном состоянии сферическую форму. Все обнаруженные на сегодня сверхтяжелые ядра (они показаны на рис. 12.5 темными ромбами) деформированы. Светлыми ромбами показаны ядра стабильные по отношению к β-распаду. Эти ядра должны распадаться в результате α-распада или деления. Основным каналом распада должен быть α-распад.
Периоды полураспада для четно-четных β-стабильных
изотопов показаны на рис. 12.6. Согласно этим предсказаниям для большинства ядер
ожидаются периоды полураспада гораздо большие, чем наблюдались для уже
обнаруженных сверхтяжелых ядер (0.1–1 мс). Так например, для ядра
292 Ds
предсказывается время жизни ~ 51 год.
Таким образом, согласно современным микроскопическим расчетам, стабильность
сверхтяжелых ядер резко возрастает по мере приближения к магическому числу по
нейтронам N = 184. До недавнего
времени единственным изотопом элемента Z = 112
Cn
(коперниций) был изотоп 277 Cn,
имеющий период полураспада 0.24 мс. Более тяжелый изотоп
283 Cn
был синтезирован в реакции холодного слияния 48 Ca + 238 U.
Время облучения 25 дней.
Полное число ионов 48 Ca на
мишени − 3.5·10 18 .
Зарегистрированы два случая, которые были интерпретированы как спонтанное
деление образовавшегося изотопа 283 Cn.
Для периода полураспада этого нового изотопа получена оценка T 1/2 = 81
c. Таким образом, видно, что увеличение числа нейтронов в изотопе
283 Cn
по сравнению с изотопом 277 Cn
на 6 единиц увеличивает время жизни на 5 порядков.
На
рис. 12.7 взятом из работы экспериментально измеренные периоды α-распада
сравниваются с результатами теоретических расчетов на основе модели жидкой капли
без учета оболочечной структуры ядер. Видно, что для всех тяжелых ядер, за
исключением лёгких изотопов урана, оболочечные эффекты увеличивают период
полураспада на 2–5 порядков для большинства ядер. Ещё более сильное влияние
оболочечная структура ядра оказывает на периоды полураспада относительно
спонтанного деления. Увеличение периода полураспада для изотопов Pu составляет
несколько порядков и увеличивается для изотопа 260 Sg.
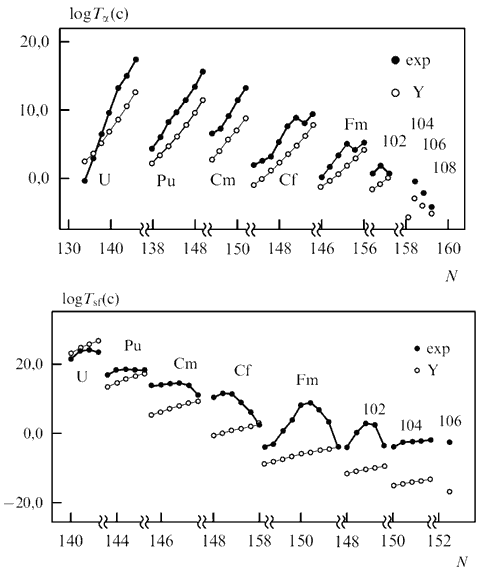
Рис. 12.7. Экспериментально измеренные (● exp) и теоретически рассчитанные (○ Y) периоды полураспада трансурановых элементов на основе модели жидкой капли без учета оболочечной структуры ядра. Верхний рисунок − периоды полураспада для α-распада, нижний рисунок − периоды полураспада для спонтанного деления.
На
рис. 12.8 показано измеренное время жизни изотопов сиборгия Sg (Z = 106) в
сравнении с предсказаниями различных теоретических моделей . Обращает на себя внимание уменьшение почти
на порядок времени жизни изотопа с N = 164 по сравнению с временем жизни изотопа
с N = 162.
Наибольшего приближения к острову стабильности можно достичь в реакции
76 Ge + 208 Pb.
Сверхтяжелое почти сферическое ядро может образоваться в реакции слияния с
последующим испусканием γ-квантов
или одного нейтрона. Согласно оценкам образующееся ядро
284 114 должно распадаться с испусканием α-частиц
с периодом полураспада ~ 1 мс. Дополнительную информацию о заполненности
оболочки в районе N = 162 можно получить, изучая α-распады
ядер 271 Hs
и 267 Sg. Для этих ядер
предсказываются периоды полураспада 1 мин. и 1 час. Для ядер
263 Sg,
262 Bh,
205 Hs,
271,273 Ds
ожидается проявление изомерии, причиной которой является заполнение подоболочек
с j = 1/2 и j = 13/2 в районе N = 162 для ядер деформированных в основном
состоянии.
На
рис. 12.9 показаны экспериментально измеренные функции возбуждения реакции
образования элементов Rf (Z = 104) и Hs (Z = 108)для реакций слияния налетающих
ионов 50 Ti и
56 Fe с ядром-мишенью 208 Pb.
Образовавшееся компаунд-ядро охлаждается испусканием одного или двух нейтронов.
Информация о функциях возбуждения реакций слияния тяжелых ионов особенно важны
для получения сверхтяжелых ядер. В реакции слияния тяжелых ионов необходимо
точно сбалансировать действие кулоновских сил и сил поверхностного натяжения.
Если энергия налетающего иона недостаточно большая, то расстояние минимального
сближения будет недостаточно для слияния двойной ядерной системы. Если энергия
налетающей частицы будет слишком большой, то образовавшаяся в результате система
будет иметь большую энергию возбуждения и с большой вероятностью произойдет
развал ее на фрагменты. Эффективно слияние происходит в довольно узком диапазоне
энергий сталкивающих частиц.
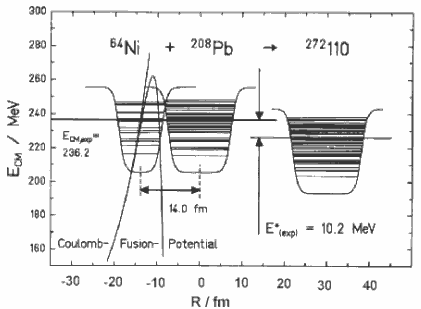
Рис.12.10. Схема потенциалов при слиянии 64 Ni
и 208 Pb.
Реакции слияния с испусканием минимального числа нейтронов (1–2) представляют
особый интерес, т.к. в синтезируемых сверхтяжелых ядрах желательно иметь
максимально большое отношение N/Z. На рис. 12.10 показан потенциал слияния для
ядер в реакции 64 Ni + 208 Pb → 272 Ds.
Простейшие оценки показывают, что вероятность туннельного эффекта для слияния
ядер составляет ~ 10 –21 , что
существенно ниже наблюдаемой величины сечения. Это можно объяснить следующим
образом. На расстоянии 14 Фм между центрами ядер первоначальная кинетическая
энергия 236.2 МэВ полностью компенсируется кулоновским потенциалом. На этом
расстоянии находятся в контакте только нуклоны, расположенные на поверхности
ядра. Энергия этих нуклонов мала. Следовательно существует высокая вероятность
того, что нуклоны или пары нуклонов покинут орбитали в одном ядре и переместятся
на свободные состояния ядра-партнера. Передача нуклонов от налетающего ядра
ядру-мишени особенно привлекательна в случае, когда в качестве мишени
используется дважды магический изотоп свинца
208 Pb. В
208 Pb заполнены протонная подоболочка h 11/2
и нейтронные подоболочки h 9/2
и i 13/2 . Вначале передача
протонов стимулируется силами притяжения протон-протон, а после заполнения
подоболочки h 9/2
- силами притяжения протон-нейтрон. Аналогично нейтроны перемещаются в свободную
подоболочку i 11/2 ,
притягиваясь нейтронами из уже заполненной подоболочки i 13/2 .
Из-за энергии спаривания и больших орбитальных моментов передача пары нуклонов
более вероятна, чем передача одного нуклона. После передачи двух протонов от
64 Ni
208 Pb кулоновский барьер
уменьшается на 14 МэВ, что способствует более тесному контакту взаимодействующих
ионов и продолжению процесса передачи нуклонов.
В
работах [В.В. Волков. Ядерные реакции глубоконеупругих передач. М. Энергоиздат,
1982; В.В. Волков. Изв. АН СССР серия физич., 1986 т. 50 с. 1879] был детально
исследован механизм реакции слияния. Показано, что уже на стадии захвата
формируется двойная ядерная система после полной диссипации кинетической энергии
налетающей частицы и нуклоны одного из ядер постепенно оболочка за оболочкой
передаются другому ядру. То есть оболочечная структура ядер играет существенную
роль в образовании компаунд-ядра. На основе этой модели удалось достаточно
хорошо описать энергию возбуждения составных ядер и сечение образования
элементов Z = 102–112
в реакциях холодного синтеза.
Таким образом, прогресс в синтезе трансурановых элементов Z = 107–112
был связан с «открытием» реакций холодного синтеза, в которых магические изотопы
208 Pb и 209 Bi
облучались ионами с Z = 22–30.
Образующееся в реакции холодного синтеза ядро нагрето слабо и охлаждается в
результате испускания одного нейтрона. Так впервые были получены изотопы
химических элементов с Z = 107–112.
Эти химические элементы были получены в период 1978–1998 гг. в Германии на
специально построенном ускорителе исследовательского центра GSI в Дармштадте.
Однако, дальнейшее продвижение − к более тяжелым ядрам − таким методом
оказывается затруднительным из-за роста величины потенциального барьера между
сталкивающимися ядрами. Поэтому в Дубне был реализован другой метод получения
сверхтяжелых ядер. В качестве мишеней использовались наиболее тяжелые изотопы
искусственно полученных химических элементов плутония Pu (Z = 94),
америция Am (Z = 95),
кюрия Cm (Z = 96),
берклия Bk (Z = 97)
и калифорния Cf
(Z = 98).
В качестве ускоренных ионов был выбран изотоп кальция
48 Ca (Z = 20).
Схематический вид сепаратора и детектора ядер отдачи показан на рис. 12.11.
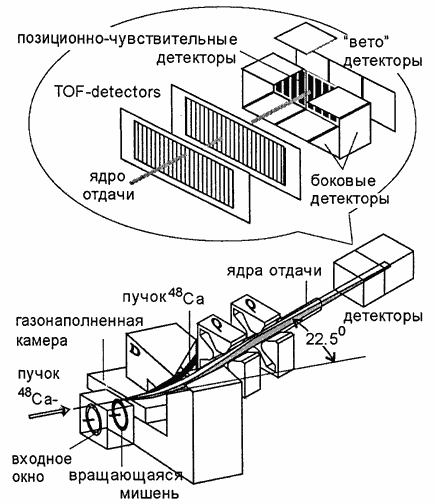
Рис. 12.11. Схематический вид сепаратора ядер отдачи, на котором проводятся
эксперименты по синтезу сверхтяжелых элементов в Дубне.
Магнитный сепаратор ядер отдачи уменьшает фон побочных продуктов реакции в 10 5 –10 7
раз. Регистрация продуктов реакции осуществлялась с помощью
позиционно-чувствительного кремниевого детектора. Измерялись энергия, координаты
и время пролета ядер отдачи. После остановки все последующие сигналы от
регистрируемых частиц распада должны исходить из точки остановки
имплантированного ядра. Созданная методика позволяла с высокой степенью
надёжности (≈ 100%)
установить связь между остановившимся в детекторе сверхтяжелым ядром и
продуктами его распада. С помощью такой методики были надёжно идентифицированы
сверхтяжелые элементы с
Z = 110–118
(табл. 12.2).
В
таблице 12.2 приведены характеристики сверхтяжелых химических элементов с Z =
110–118: массовое число A,
m − наличие изомерного состояния
в изотопе с массовым числом A,
спин-четность J P ,
энергия связи ядра E св,
удельная энергия связи ε,
энергии отделения нейтрона
B n
и протона B p ,
период полураспада
T 1/2
и основные каналы распада.
Химические элементы Z > 112
пока не имеют названий и приводятся в принятых международных обозначениях.
Таблица 12.2
Характеристики сверхтяжелых химических элементов Z = 110–118
| XX-A-m | J P | Масса ядра, MэВ |
E св, MэВ |
ε, MэВ |
B n , MэВ |
B p , MэВ |
T 1/2 | Моды распада |
|---|---|---|---|---|---|---|---|---|
| Z = 110 − дармштадтий | ||||||||
| Ds-267 | 248787.19 | 1934.5 | 7.2 | 0.7 | 2.8 ас | α ≈100% | ||
| Ds-268 | 0 + | 249718.08 | 1943.2 | 7.3 | 8.7 | 1.3 | 100 ас | α ≈ |
| Ds-269 | 250650.86 | 1950.0 | 7.2 | 6.8 | 1.3 | 179 ас | α 100% | |
| Ds-270 | 0 + | 251581.97 | 1958.4 | 7.3 | 8.5 | 0.10 мс | α ≈100%, SF < 0.20% | |
| Ds-270-m | 251583.07 | 1957.3 | 7.2 | 6.0 мс | α >70%, IT ≤ 30% | |||
| Ds-271 | 252514.72 | 1965.2 | 7.3 | 6.8 | 2.2 | 1.63 мс | α ≈100% | |
| Ds-271-m | 252514.72 | 1965.2 | 7.3 | 69 мс | IT?, α >0% | |||
| Ds-272 | 0 + | 253446.46 | 1973.1 | 7.3 | 7.8 | 2.5 | 1 с | SF |
| Ds-273 | 254380.32 | 1978.8 | 7.2 | 5.7 | 2.5 | 0.17 мс | α ≈100% | |
| Ds-274 | 0 + | 255312.45 | 1986.2 | 7.2 | 7.4 | 3.0 | 2 с | α?, SF? |
| Ds-275 | 256246.44 | 1991.8 | 7.2 | 5.6 | 2.9 | 2 с | α? | |
| Ds-276 | 0 + | 257178.73 | 1999.1 | 7.2 | 7.3 | 3.2 | 5 с | SF?, α? |
| Ds-277 | 258112.63 | 2004.7 | 7.2 | 5.7 | 3.1 | 5 с | α? | |
| Ds-278 | 0 + | 259044.92 | 2012.0 | 7.2 | 7.3 | 10 с | SF?, α? |
|
| Ds-279 | 259978.62 | 2017.9 | 7.2 | 5.9 | 0.18 с | SF
≈90%, α ≈10% |
||
| Ds-281 | 261844.60 | 2031.0 | 7.2 | 9.6 с | SF ≈100% | |||
| Z =111 − рентгений | ||||||||
| Rg-272 | 253452.75 | 1965.5 | 7.2 | 0.2 | 3.8 мс | α ≈100% | ||
| Rg-273 | 254384.34 | 1973.5 | 7.2 | 8.0 | 0.4 | 5 мс | α? | |
| Rg-274 | 255317.74 | 1979.6 | 7.2 | 6.2 | 0.9 | 6.4 мс | α ≈100% | |
| Rg-275 | 256249.53 | 1987.4 | 7.2 | 7.8 | 1.2 | 10 мс | α? | |
| Rg-276 | 257183.22 | 1993.3 | 7.2 | 5.9 | 1.5 | 100 мс | SF?, α? |
|
| Rg-277 | 258115.72 | 2000.4 | 7.2 | 7.1 | 1.3 | 1 с | α?, SF? |
|
| Rg-278 | 259049.11 | 2006.5 | 7.2 | 6.2 | 1.8 | 4.2 мс | α
≈100%, SF |
|
| Rg-279 | 259981.41 | 2013.8 | 7.2 | 7.3 | 1.8 | 0.17 с | α ≈100% | |
| Rg-280 | 260914.80 | 2020.0 | 7.2 | 6.2 | 2.1 | 3.6 с | α ≈100% | |
| Rg-281 | 261847.09 | 2027.2 | 7.2 | 7.3 | 1 м | α?, SF? | ||
| Rg-282 | 262780.59 | 2033.3 | 7.2 | 6.1 | 2.3 | 4 м | SF?, α? | |
| Rg-283 | 263712.98 | 2040.5 | 7.2 | 7.2 | 10 м | SF?, α? | ||
| Z = 112 − коперниций | ||||||||
| Cn-277 | 258119.32 | 1995.5 | 7.2 | 2.2 | 0.69 мс | α ≈100% | ||
| Cn-278 | 0 + | 259051.20 | 2003.1 | 7.2 | 7.7 | 2.8 | 10 мс | SF?, α? |
| Cn -279 | 259984.69 | 2009.2 | 7.2 | 6.1 | 2.7 | 0.1 с | SF?, α? | |
| Cn -280 | 0 + | 260916.69 | 2016.8 | 7.2 | 7.6 | 3.0 | 1 с | α?, SF? |
| Cn -282 | 0 + | 262782.18 | 2030.4 | 7.2 | 3.2 | 0.50 мс | SF ≈100% | |
| Cn -283 | 263715.57 | 2036.6 | 7.2 | 6.2 | 3.3 | 4.0 с | α ≥90%, SF ≤10% | |
| Cn -284 | 0 + | 264647.66 | 2044.1 | 7.2 | 7.5 | 3.6 | 101 мс | SF ≈100% |
| Cn -285 | 265580.76 | 2050.5 | 7.2 | 6.5 | 34 с | α ≈100% | ||
| Z = 113 | ||||||||
| Uut-278 | 0.24 мс | α 100% | ||||||
| Uut-283 | 263719.46 | 2031.4 | 7.2 | 1.0 | 100 мс | α 100% | ||
| Uut-284 | 264652.45 | 2038.0 | 7.2 | 6.6 | 1.4 | 0.48 с | α ≈100% | |
| Uut-285 | 265584.55 | 2045.5 | 7.2 | 7.5 | 1.4 | 2 м | α?, SF? | |
| Uut-286 | 266517.64 | 2051.9 | 7.2 | 6.5 | 1.4 | 5 м | α?, SF? | |
| Uut-287 | 267449.64 | 2059.5 | 7.2 | 7.6 | 20 м | α?, SF? | ||
| Z = 114 | ||||||||
| Uuq-286 | 0 + | 266520.33 | 2048.0 | 7.2 | 2.5 | 0.16 с | SF ≈60%, α ≈40% | |
| Uuq-287 | 267453.42 | 2054.4 | 7.2 | 6.5 | 2.5 | 0.51 с | α ≈100% | |
| Uuq-288 | 0 + | 268385.02 | 2062.4 | 7.2 | 8.0 | 2.9 | 0.80 с | α ≈100% |
| Uuq-289 | 269317.91 | 2069.1 | 7.2 | 6.7 | 2.7 с | α ≈100% | ||
| Z = 115 | ||||||||
| Uup-287 | 267458.11 | 2048.4 | 7.1 | 0.5 | 32 мс | α 100% | ||
| Uup-288 | 268390.81 | 2055.3 | 7.1 | 6.9 | 0.9 | 87 мс | α 100% | |
| Uup-289 | 269322.50 | 2063.2 | 7.1 | 7.9 | 0.8 | 10 с | SF?, α? | |
| Uup-290 | 270255.30 | 2070.0 | 7.1 | 6.8 | 0.9 | 10 с | SF?, α? | |
| Uup-291 | 271187.09 | 2077.7 | 7.1 | 7.8 | 1 м | α?, SF? | ||
| Z = 116 | ||||||||
| Uuh-290 | 0 + | 270258.98 | 2065.0 | 7.1 | 1.8 | 15 мс | α ≈100% | |
| Uuh-291 | 271191.78 | 2071.7 | 7.1 | 6.8 | 1.8 | 6.3 мс | α 100% | |
| Uuh-292 | 0 + | 272123.07 | 2080.0 | 7.1 | 8.3 | 2.3 | 18 мс | α ≈100% |
| Uuh-293 | 53 мс | α ≈100% | ||||||
| Z = 117 | ||||||||
| Uus-291 | 271197.37 | 2064.9 | 7.1 | -0.1 | 10 мс | SF?, α? | ||
| Uus-292 | 272129.76 | 2072.0 | 7.1 | 7.2 | 0.3 | 50 мс | SF?, α? | |
| Z = 118 | ||||||||
| Uuo-294 | 0 + | 1.8 мс | α ≈100% | |||||
На рис. 12.12 показаны все известные наиболее тяжелые изотопы с Z = 110–118, полученные в реакциях синтеза с указанием экспериментально измеренного периода полураспада. Здесь же показано теоретически предсказанное положение острова стабильности (Z = 114, N = 184).

Рис. 12.12. N-Z-диаграмма
элементов Z = 110–118.
Полученные результаты однозначно указывают на рост стабильности изотопов при
приближении к дважды магическому ядру (Z = 114,
N = 184).
Добавление к ядрам с Z = 110
и 112 7–8 нейтронов увеличивает период полураспада от 2.8 ас (Ds-267)
до ≈ 10 с (Ds-168, Ds 271). Период полураспада T 1/2 (272 Rg, 273 Rg) ≈ 4–5
мс увеличивается до T 1/2 (283 Rg) ≈ 10 мин. Наиболее тяжелые изотопы элементов
Z = 110–112
содержат ≈ 170 нейтронов,
что ещё далеко от магического числа N = 184.
Все наиболее тяжелые изотопы с Z > 111
и
N > 172
распадаются преимущественно в результате
α-распада,
спонтанное деление – более редкий распад. Эти результаты находятся в хорошем
согласии с теоретическими предсказаниями.
В
Лаборатории ядерных реакций им. Г.Н. Флерова (Дубна) синтезирован элемент с
Z = 114. Была использована реакция
Идентификация ядра 289 114
проводилась по цепочке α-распадов.
Экспериментальная оценка периода полураспада изотопа
289 114 ~30 с. Полученный результат находится в хорошем
согласии с ранее выполненными расчетами .
При синтезе 114 элемента в реакции 48 Cu + 244 Pu
максимальный выход изотопов с
Z = 114
наблюдался в канале с испарением трех нейтронов. При этом энергии возбуждения
составного ядра 289 114 была
35 МэВ.
Теоретически предсказываемая последовательность распадов, происходящих с ядром
296 116, образующемся в
реакции
248 Cm + 48 Ca → 296 116,
приведена на рис.12.13

Рис. 12.13. Схема распада ядра 296 116.
Изотоп 296 116 охлаждается в результате испускания четырех нейтронов и превращается в изотоп 292 116, который далее с 5% -ой вероятностью в результате двух последовательных e-захватов превращается в изотоп 292 114. В результате α-распада (T 1/2 = 85 дней) изотоп 292 114 превращается в изотоп 288 112. Образование изотопа 288 112 происходит и по каналу
Конечное ядро 288 112,
образующееся в результате обеих цепочек, имеет период полураспада около 1 часа и
распадается в результате спонтанного деления. Примерно с 10%-ой вероятностью в
результате α-распада
изотопа 288 114 может
образовываться изотоп 284 112.
Приведенные выше периоды и каналы распада получены расчетным путем.
На
рис. 12.14 приведена цепочка последовательных α-распадов
изотопа 288 115,
измеренная в экспериментах в Дубне. ER
− энергия ядра отдачи, имплантированного в позиционно-чувствительный кремниевый
детектор. Можно отметить хорошее совпадение в периодах полураспада и энергиях α-распадов
в трёх экспериментах, что свидетельствует о надёжности метода идентификации
сверхтяжелых элементов с помощью измерений спектров α-частиц.

Рис. 12.14. Цепочка
последовательных α-распадов
изотопа 288 115,
измеренная в экспериментах в Дубне.
Самый тяжелый, полученный в лабораторных условиях элемент с Z = 118, был синтезирован в реакции
48 Ca + 249 Cf → 294 118 + 3n.
При энергии ионов вблизи кулоновского барьера наблюдалось три случая образования
118 элемента. Ядра 294 118
имплантировались в кремниевый детектор и наблюдалась цепочка последовательных α-распадов.
Сечение образования 118 элемента составляло ~2 пикобарна. Период полураспада
изотопа 293 118 равен 120 мс.
На
рис. 12.15 показана теоретически рассчитанная цепочка последовательных α-распадов
изотопа 293 118 и приведены
периоды полураспада дочерних ядер, образующихся в результате α-распадов.

Рис. 12.15. Цепочка последовательных α-распадов
изотопа 293 118.
Приведены средние времена жизни дочерних ядер, образующихся в результате α-распадов.
Анализируя различные возможности образования сверхтяжелых элементов в реакциях с тяжелыми ионами нужно учитывать следующие обстоятельства.
- Необходимо создать ядро с достаточно большим отношением числа нейтронов к числу протонов. Поэтому в качестве налетающей частицы надо выбирать тяжелые ионы, имеющие большое N/Z.
- Необходимо, чтобы образующееся компаунд-ядро имело малую энергию возбуждения и небольшую величину момента количества движения, так как в противном случае будет снижаться эффективная высота барьера деления.
- Необходимо, чтобы образующееся ядро имело форму близкую к сферической, так как даже небольшая деформация будет приводить к быстрому делению сверхтяжелого ядра.
Весьма перспективным методом получения сверхтяжелых ядер являются реакции типа 238 U + 238 U, 238 U + 248 Cm, 238 U + 249 Cf, 238 U + 254 Es. На рис. 12.16 приведены оценочные сечения образования трансурановых элементов при облучении ускоренными ионами 238 U мишеней из 248 Cm, 249 Cf и 254 Es. В этих реакциях уже получены первые результаты по сечениям образования элементов с Z > 100. Для увеличения выходов исследуемых реакций толщины мишеней выбирались таким образом, чтобы продукты реакции оставались в мишени. После облучения из мишени сепарировались отдельные химические элементы. В полученных образцах в течение нескольких месяцев регистрировались продукты α-распада и осколки деления. Данные, полученные с помощью ускоренных ионов урана, ясно указывают на увеличение выхода тяжелых трансурановых элементов по сравнению с более легкими бомбардирующими ионами. Этот факт чрезвычайно важен для решения проблемы синтеза сверхтяжелых ядер. Несмотря на трудности работы с соответствующими мишенями прогнозы продвижения к большим Z выглядят довольно оптимистично.

Рис. 12.16. Оценки сечений образования трансурановых элементов в реакциях
238 U с
248 Cm,
249 Cf и 254 Es
Продвижение в область сверхтяжелых ядер в последние годы оказалось ошеломляюще
впечатляющим. Однако все попытки обнаружить Остров Стабильности пока не
увенчались успехом. Поиск его интенсивно продолжается.
Оболочечная структура атомных ядер играет существенную роль в повышении
стабильности сверхтяжелых ядер. Магические числа Z ≈ 114
и
N ≈ 184,
если они действительно существуют, могут привести к значительному повышению
стабильности атомных ядер. Существенным является также то, что распад
сверхтяжелых ядер будет происходить в результате α-распада,
что важно для разработки экспериментальных методов детектирования и
идентификации новых сверхтяжелых ядер.
Современную материально-техническую базу производства примерно на 90% составляют всего лишь два вида материалов: металлы и керамика. В мире ежегодно производится около 600 млн. т металла - свыше 150 кг. на каждого жителя планеты. Примерно столько же производится керамики вместе с кирпичом. Изготовление металла обходится в сотни и тысячи раз дороже, производство керамики намного легче в техническом отношении и выгоднее экономически, и, главное, керамика во многих случаях оказывается более подходящим конструкционным материалом по сравнению с металлом.
С применением новых химических элементов - циркония, титана, бора, германия, хрома, молибдена, вольфрама и т.д. в последнее время синтезируют огнеупорную, термостойкую, химостойкую, высокотвердую керамику, а также керамику с набором заданных электрофизических свойств.
Сверхтвердый материал - гексанит-Р как одна из кристаллических разновидностей нитрида бора, с температурой плавления свыше 3200 0 С и твердостью, близкой к твердости алмаза, обладает рекордно высокой вязкостью, т. е. он не так хрупок, как все другие керамические материалы. Решена, таким образом, одна из труднейших научно-технических проблем века: до сих пор всей конструкционной керамике был присущ общий недостаток - хрупкость, теперь же сделан шаг к его преодолению.
Большое преимущество технической керамики нового состава в том, что детали машин из нее производятся прессованием порошков с получением готовых изделий заданных форм и размеров.
Сегодня можно назвать еще одно уникальное свойство керамики - сверхпроводимость при температурах выше температуры кипения азота, это свойство открывает невиданные просторы для научно-технического прогресса, для создания сверхмощных двигателей и электрогенераторов, создания транспорта на магнитной подушке, разработки сверхмощных электромагнитных ускорителей для вывода полезных грузов в космосе и т.д.
Химия кремнийорганических соединений позволила создать многотоннажное производство самых разнообразных полимеров, обладающих огнезащитными, водоотталкивающими, электроизоляционными и другими ценными свойствами. Эти полимеры незаменимы в ряде отраслей энергетики и авиапромышленности.
Фтороуглероды - тетравторметан, гексафторэтан и их производные, где атом углерода несет слабый положительный заряд, а атом фтора с присущей фтору электроотрицательностью - слабый отрицательный заряд. В результате фтороуглероды обладают исключительной устойчивостью даже в очень агрессивных средах кислот и щелочей, особой поверхностной активностью, способностью поглощать кислород и перекиси. Поэтому они применяются в качестве материала для протезов внутренних органов человека.
Вопрос 57. Химические процессы и процессы жизнедеятельности. Катализаторы и ферменты.
Интенсивные исследования последнего времени направлены на выяснение как материального состава растительных и животных тканей, так и химических процессов, происходящих в организме. Идея о ведущей роли ферментов, впервые предложенная великим французским естествоиспытателем Луи Пастером (1822-1895), остается основополагающей и по сей день. В то же время изучением молекулярного состава и структуры ткани живого и неживого организма занимается статическая биохимия.
Динамическая биохимия родилась на рубеже XVIII и XIX столетий, когда начали различать процессы дыхания и брожения, ассимиляции и диссимиляции как некие превращения веществ.
Исследование брожения составляет основной предмет ферментологии - стержневой отрасли знаний о процессах жизнедеятельности. На протяжении весьма длительной истории исследования процесс биокатализа рассматривался с двух разных точек зрения. Одной из них, условно названной химической, придерживались Ю. Либих и М. Бертло, а другой - биологической - Л. Пастер.
В химической концепции весь катализ сводился к обычному химическому катализу. Несмотря на упрощенный подход в рамках концепции были установлены важные положения: аналогия между биокатализом и катализом, между ферментами и катализаторами; наличие в ферментах двух неравноценных компонентов - активных центров и носителей; заключение о важной роли ионов переходных металлов и активных центров многих ферментов; вывод о распространении на биокатализ законов химической кинетики; сведение в отдельных случаях биокатализа к катализу неорганическими агентами.
В начале развития биологическая концепция не располагала столь обширными экспериментальными подтверждениями. Ее основной опорой были труды Л. Пастера и, в частности, его прямые наблюдения за деятельностью молочнокислых бактерий, которые позволили выявить брожение и способность микроорганизмов получать необходимую им энергию для жизнедеятельности путем брожения. Из своих наблюдений Пастер сделал вывод об особом уровне материальной организации ферментов. Однако все его доводы, если и были не опровергнуты, то по крайней мере отодвинуты на задний план после открытия внеклеточного брожения, а позиция Пастера была объявлена виталистической.
Однако с течением времени концепция Пастера победила. О перспективности данной концепции свидетельствуют современные эволюционный катализ и молекулярная биология. С одной стороны, установлено, что состав и структура биополимерных молекул представляют собой единый набор для всех живых существ, вполне доступный для исследования физических и химических свойств - одни и те же физические и химические законы управляют как абиогенными процессами, так и процессами жизнедеятельности. С другой стороны, доказана исключительная специфичность живого, проявляющаяся не только в высших уровнях организации клетки, но и в поведении фрагментов живых систем на молекулярном уровне, на котором отражаются закономерности других уровней. Специфичность молекулярного уровня живого заключается в существенном различии принципов действия катализаторов и ферментов, в различии механизмов образования полимеров и биополимеров, структура которых определяется только генетическим кодом и, наконец, в своем необычном факте: многие химические реакции окисления-восстановления в живой клетке могут происходить без непосредственного контакта между реагирующими молекулами. А это означает, что в живых системах могут происходить такие химические превращения, которые не обнаруживались в неживом мире.
Ранее в 2011 году IUPAC признал за коллаборацией ОИЯИ с LLNL (США) приоритет в открытии 114 и 116 элементов, которые получили названия: 114 элемент ― Flerovium, Fl; 116 элемент ― Livermorium, Lv.
Флеровий ― в честь Лаборатории ядерных реакций им. Г.Н.Флерова ОИЯИ, являющейся признанным лидером в области синтеза сверхтяжелых элементов, и ее основателя выдающегося физика академика Г.Н.Флерова (1913−1990) ― автора открытия нового вида радиоактивности спонтанного деления тяжелых ядер, основоположника ряда новых научных направлений, основателя и первого директора ЛЯР ОИЯИ, которая сейчас носит его имя.
Ливерморий ― в честь Ливерморской национальной лаборатории им. Лоуренса и места ее расположения ― города Ливермор (штат Калифорния, США). Ученые Ливермора уже более 20-ти лет участвуют в проводимых в Дубне экспериментах по синтезу новых элементов.
В целом решение IUPAC является признанием выдающегося вклада ученых ОИЯИ в открытие «острова стабильности» сверхтяжелых элементов, что является одним из важнейших достижений современной ядерной физики.
≪ Химическая эра≫ в химиотерапии началась вместе с развитием
обрабатывающей промышленности. Гениальный анализ
Маркса и Ленина показывает нам, как протекал процесс
развития капитализма в промышленности: от простой кооперации
труда через мануфактуру (в XVI-VII веке) промышленность
в конце XVIII и начале XIX века перешла к капиталистической
фабрике, т. е. к крупному машинному производству.
Ручной труд вытеснялся машинным.
Паровые машины, развитие железнодорожного и водного
парового транспорта, машинное прядение, новые способы
литья чугуна и стали -все это вызвало революцию в промышленности.
Наступила эпоха промышленного переворота.
Химическая наука едва поспевала за требованиями механической
промышленности. В области теории эта наука сделала
крупный скачок вперед в середине XVIII века.
Основы научной химии и термодинамики заложил наш
знаменитый соотечественник Ломоносов.
В 1748 году в известном письме к математику Эйлеру - члену Российской академии наук -Ломоносов впервые сформулировал
закон постоянства материи и движения. Ему же
принадлежит и вторая важнейшая заслуга: он пропагандировал
идею о необходимости изучить проблему атомного и
молекулярного строения материи, ибо от этого строения зависят
свойства всех тел, их химическая и физическая природа.
≪ ...Химия, -писал Ломоносов в Слове о пользе химии,
Первая предводительница будет в раскрытии внутренних
чертогов тел, первая проникнет во внутренние тайники
тела, первая позволит познакомиться с ч а с т и ч к а м и ≫ .
≪ Широко простирает химия руки свои в дела человеческие
≫ -таким словом закончил он один из отделов этого
≪ Слова≫ . ≪ Непрерывное рождение и разрушение тел достаточно
красноречиво говорит о движении корпускулой≫ , писал
мертвых, движутся в растениях -живых и мертвых, в минералах
или в неорганическом, следовательно, во всем≫ .
Механизация ткацкого производства вызвала необходимость
революции в механике и химии ситцепечатного и красильного
дела, обработка же металлов, их упрочнение потребовали
глубокого вмешательства химических элементов в процесс
Несомненно, основными достижениями химии современная
наука обязана трем гениальным русским химикам -Николаю
Николаевичу Зинину, Александру Михайловичу Бутлерову я
Дмитрию Ивановичу Менделееву.
Профессор Казанского университета Н. Н. Зинин в 1841
году путем химического синтеза получил из циклического соединения
нитробензола анилин -исходный продукт, из которого
путем обработки получаются десятки различных красителей.
До этого краски готовились из растительных продуктов.
Зинин по справедливости считается отцом так называемой
с и н т е т и ч е с к о й химии.
Если бы Зинин не сделал ничего более, кроме превращения
нитробензола в анилин, то имя его и тогда вошло бы в
историю науки как имя величайшего химика. Синтез анилина
открыл новую эру в химической и лекарственной промышленности.
Воздействуя на анилин соляной кислотой, метиловым спиртом,
фосгеном и другими реактивами, можно получить очень
большое число красителей для тканей. Более двухсот красителей
производит советская химическая промышленность из
бесцветного анилина. Анилин используется при производстве
фильмов, а также проявителей для цветных фильмов. Из анилина
получается вещество, ускоряющее процесс вулканизации
резины. Более ста лекарственных препаратов, изготовляемых
в настоящее время, в том числе стрептоцид и сульфаниламиды,
являются производными анилина.
Ясный ум Ломоносова еще в XVIII веке предвидел значение
химии для медицины: ≪ Медик без довольного знания химии
совершен быть не может...≫ ; ≪ от одной химии уповать
можно на исправление недостатков врачебной науки...≫ .
Преемник Зинина А. М. Бутлеров совершил революцию в
учении о строении органических химических соединений.
Убежденный в реальности атомов, Бутлеров поставил целью
выразить точными формулами химические связи между атомами,
образующими молекулу органического соединения. Бутлеров
считал, что можно выяснить строение молекул и с помощью
физических методов, и путем химических превращений.
Идя по этому пути, он разработал свою теорию химического
строения органических соединений. После настойчивых опытов
с бутильными спиртами Бутлеров установил, что одно и
то же количество определенных атомов (например, углерода,
водорода и кислорода), находящихся в цепном соединении,
может давать различные продукты и что свойства получаемых
химических продуктов зависят от того, в каком порядке будут
связаны элементы друг с другом. Это увеличило как число
возможных комбинаций при синтезе новых химических веществ,
так и количество лечебных препаратов, получаемых
путем химического синтеза.
Величайшее открытие XIX века -периодический закон
Менделеева - . привело к установлению строгого порядка и
закономерности среди химических элементов. Мерилом этой
закономерности стал атомный вес. Многие химиопрепараты в
прошлом открывались случайно. Но наука -враг случайного.
По мере прогресса научных знаний многое, казавшееся таинственным
и непостижимым, стало ясным и закономерным.
Периодический закон Менделеева поставил всю химическую
науку и, в частности, химиотерапию на прочную научную основу.
≪ До периодического закона, -писал Менделеев, - . простые
тела представляли лишь отрывочные, случайные явления
природы: не было поводов ждать каких-либо новых, а вновь
находимые в своих свойствах были полной неожиданной новинкой.
Периодическая законность первая дала возможность
видеть не открытые еще элементы в такой дали, до которой не
вооруженное этой закономерностью химическое зрение до тех
пор не достигало, а при этом новые элементы, ранее их открытые,
рисовались с целой массой свойств≫ 1.
Недаром Энгельс охарактеризовал научное предвидение
Менделеева как научный подвиг. Это действительно была выдающаяся
победа науки о химических явлениях, победа позволившая
человечеству встать на прочный путь освобождения
от власти случайностей и подчинения себе сил природы. Периодическая
система Менделеева позволила найти целую
группу близких друг другу химических элементов, полезных
для лечения многих болезней (мышьяк, ртуть, сурьма).
Эти элементы явились для ученых конца XIX века как
бы золотой жилой. При этом ученые полностью использовали
зининский принцип химического синтеза и бутлеровские комбинации
в расположении атомов и молекул.
Среди ученых медиков, занявшихся изготовлением синтетических
лекарств, наибольший успех выпал на долю Эрлиха.
Вся жизнь Эрлиха была посвящена настойчивому осуществлению
одной идеи -получить путем химического соединения
не вредя организму.
Важно подчеркнуть, что эту мысль в 1891 году высказал
основоположник химиотерапии Д. Л. Романовский. Он писал,
что считает идеальным лекарством ≪ вещество, которое при
введении в заболевший организм окажет наименьший вред
последнему и вызовет наибольшее деструктивное изменение в
поражающем агенте≫ . Романовский предвосхитил идею Эрли-
ха о ≪ волшебных пулях≫ , легко попадающих во врагов. Романовский
первый на основе точных наблюдений установил
важнейший закон химиотерапии -прямой механизм действия
химического лекарства на возбудителя болезни.
≪ Хинин при введении в организм малярика в достаточной
легко наблюдаемые деструктивные изменения, главным
образом -его ядра, почему этот препарат нужно считать истинным
специфическим лекарством против малярии≫ .
сказывается специфичность этого средства при малярии - истинная специфичность действия на самую сущность болезни,
Романовский первый поставил вопрос о ≪ радикальном действии
≫ химиопрепаратов на возбудителей или, как он выразился,
≪ производителей≫ болезни. Таким образом, он был зачинателем
идеи в е л и к о й с т е р и л и з у ю щ е й т е р а п и и.
Если существует в природе хинин, -рассуждал вслед за
для организма человека, то должны быть и другие
подобные вещества, которыми можно победить остальные болезни.
В конце XIX века химическая наука продолжала свое
триумфальное шествие, начатое Ломоносовым и завершенное
Зининым, Бутлеровым и Менделеевым.
Журналы были переполнены новыми и интереснейшими
сообщениями о завоевании химии.
Однако с чего начать? Какое вещество из сотен уже полученных
химически может быть использовано для синтеза
химиопрепарата?
Еще в студенческие годы Эрлих повторил известный опыт
киевского профессора Гейбеля, который доказал, что при
отравлении свинцом этот металл неравномерно распределяется
в организме: в одних органах свинец скапливается в заметных
количествах, в трупе же его не удается обнаружить даже тончайшими
реактивами. Значит, химические вещества обладают
избирательным действием, решил Эрлих.
Однако Эрлих отказался от опытов со свинцом, ибо на
глаз отравленные клетки ничем не отличались от здоровых.
Он остановился на краске -метиленовой синьке, так как она
будет удобнее для наблюдения, и предложил лечить малярию
метиленовой синькой. Это лечение дало кое-какие результаты.
Эрлих был ободрен ими и стал расширять свои опыты.
узкий листок с хвостиком и вызывающих у лошадей
мышам и вызывали у них смертельное заболевание.
Эрлих засел в лаборатории и стал проверять краски на
зараженных мышах. Это был, возможно, упрощенный способ,
но таковы были первые шаги научной химиотерапии. Трудно
сразу установить, какая краска имеет в условиях животного
От одной краски мыши синели, от другой -желтели, а
хвостатые трипаносомы попрежнему плавали в кровяном русле
мышей и убивали их. С красками ровно ничего не выходило.
В естествознании ≪ золотые крупинки истины≫ рождаются
из ≪ тысяч тонн переработанной руды≫ . Надо только открыть
какое-либо средство, а там химик расчленит его, добавит
кислоту или щелочь, соединит с реактивами, определит атомный
вес, испытает на больных животных, а потом на людях...
И тогда в таблице лечебных химиопрепаратов появляется
новое спасительное средство.
Трудно было пробиваться к рациональной химиотерапии.
Надо было искать компас, который должен вывести на правильный
путь. Надо было искать закономерности...
И вот однажды, сидя в своем кабинете, Эрлих прочитал в
свежем номере химического журнала о новом патентованном
средстве. Оно называлось ≪ атоксил≫ , что означает нетоксичный.
Начались испытания этого средства на мышах, зараженных
трипаносомами.
После сотен опытов можно было отметить, что атоксил
действительно излечивает мышей.
Но некоторые мыши все же погибали. Следовательно, не
так уже атоксил безвреден.
Эрлих решил сделать его безвредным. Это средство стоило
того, чтобы над ним поработать.
В состав атоксила входило то же бензольное кольцо, что
и в некоторые краски.
Бензольное кольцо -это шесть атомов углерода, сцепленных
в один круг. Но к нему была добавлена окись мышьяка.
Это, очевидно, и сделало препарат целебным. Мышьяк -известный
яд, но при соединении его с бензольным кольцом
получилось химиотерапевтическое средство.
Однако надо было больше ≪ облагородить≫ этот яд, превратив
его в еще более безопасное и в то же время сильно действующее
на возбудителей болезни средство.
атоксил, заявили, что изменить атоксил нельзя, он тут же
распадется. Однако Эрлиху удалось видоизменить этот препарат
в сотни препаратов мышьяка, совершенно не нарушая
комбинации бензола с мышьяком.
Два года проработал он в своей лаборатории, пока не
открыл такое средство, которое совершенно очищало кровь
мышей от убивавших их свирепых трипаносом. При этом новое
средство оказалось безвредным для мышей. Они хорошо переносили
≪ 606≫ или сальварсан, -так был назван новый препарат,
ибо он был 606-м вариантом атоксила. Этот препарат являлся
продуктом тончайшего химического синтеза, и его приготовление
было сопряжено с опасностью взрыва и пожара ввиду
большого количества участвующих в реакции соединения
эфирных паров.
А самое главное -удалось установить, что препарат надо
сохранять в безвоздушной ампуле -примесь воздуха делает
его ядовитым.
Таков был препарат, носивший химическое название: диок-
си-диамино-арсенобензол-дигидро-хлорид.
Но тут произошло одно знаменательное событие.
Незадолго до исследования Эрлиха известный ученый Шау.
дин открыл возбудителя сифилиса -бледную спирохету, происходящую
из семейства трипаносом.
Но, подумал Эрлих, нельзя же останавливаться на лошадиных
трипаносомах, надо воздействовать и на спирохету,
поражающую человека.
Однако он не сразу перешел на людей; он заразил сифилисом
кроликов, а затем лечил их препаратом ≪ 606≫ . После
нескольких вливаний у кроликов не оставалось ни одной
спирохеты. На кроликах вырабатывались и дозы препарата.
Эрлих произвел еще 308 соединений и получил более совершенный
препарат -≪ 914≫ (неосальварсан). Этот препарат
растворялся в 5 кубических сантиметрах воды. Его введение
в организм оказалось еще более безопасным: реакции бывали
Препараты все же сохранили какие-то ядовитые свойства.
У отдельных больных, особенно при введении повышенных доз,
препараты ≪ 606≫ и ≪ 914≫ вызывали воспаление мозга, потерю
сознания, повышение температуры, кожные кровоизлияния.
Враги Эрлиха подняли шумиху вокруг новых препаратов.
Немало волнений доставили они Эрлиху.
Когда препараты Эрлиха были проверены на большом количестве
больных, выяснилось, что ядовитое действие они оказывают
крайне редко.
Весь мир признал огромное значение новых средств.
Сифилис перестал быть страшной болезнью. Лечение давало
прекрасные результаты; язвы у больных исчезали после
нескольких вливаний.
Эрлих решил покончить и со спирохетой возвратного тифа,
родственной сифилитической спирохете.
В это время в некоторых городах России наблюдались
вспышки возвратного тифа. Русские врачи Ю. Ю. Иверсен в
Петербурге и П. К. Галлер в Саратове приняли смелое решение
и первые в мире поставили широкое испытание нового
препарата на больных возвратным тифом.
Эффект лечения был поразительный: после того как больному
при температуре 40° вливалось полграмма эрлиховского
препарата, через 14-6 часов начинался сильнейший пот и
температура падала совсем. Больной совершенно выздоравливал.
Организм его полностью освобождался от спирохет.
Разве это не осуществление мечты ученых о великой стерилизующей
После нескольких лет применения сальварсана русские ученые
установили, что после вливаний сальварсана наблюдаются
лишь небольшие реакции, а смертельные осложнения наступают
крайне редко (на 100 000 вливаний один смертельный исход).
Улучшение качества препарата, установление правильных
доз и точных противопоказаний, -писали в 1916-917
годах наши ученые Г. И. Мещерский, С. Л. Богров и В. В. Ива.
нов, -приведут к тому, что это средство будет совершенно
безопасным.
Передовые русские исследователи-химики и врачи вскоре
после открытия Эрлиха поставили перед собой задачу изготовить
отечественный сальварсан.
Химиком В. А. Смирновым в фармацевтической лаборатории В. К. Ферейна
уже в 1914 году был получен хороший, нетоксичный препарат типа
сальварсана. Единственным его недостатком было несколько сниженное
мышах, произведенного Я. Г. Шерешевским, С. Л. Богровым,
С. С. Усольцевым и др., новый препарат, который получил название ≪ бен-
зарсан≫ , стали применять в клиниках для лечения больных. Профессор
Т. П. Павлов, Г. И. Мещерский и В. В. Иванов в ряде статей, опубликованных
в 1916-917 годах в ≪ Русском враче≫ , ≪ Врачебной газете≫ и
≪ Русском журнале кожных и венерических болезней≫ , дали о первом русском
сальварсане отличный отзыв.
В дальнейшем, с 1916 года, было организовано массовое фабричное
производство русского сальварсана. Это производство возглавил известный
русский химик П. Ф. Рюмшин, разработавший оригинальную общепризнанную
технологию синтеза сальварсана.
Одновременно со Смирновым русский сальварсан (под названием ≪ ар-
Ол≫ ) синтезировали в 1914 году московские химики И. И. Остромыслен-
ский и С. С. Келбасинский.
В 1915 году в ≪ Русском журнале кожных и венерических болезней≫
появился весьма благоприятный отзыв Богрова и Мещерского об этом
препарата.
После Великой Октябрьской социалистической революции было налажено
производство русского сальварсана (новарсалана, новарсола)в заводских





