Для наименования органических соединений используется несколько систем, но ни одна из них не подходит для всех соединений. Сохранились многие тривиальные названия, которые либо применялись еще в начальный период органической химии и отражают источник получения или характерные качества, либо являются более новыми несистематическими названиями, которые используются по причине удобства. Так, спирт CH 3 OH иногда называют «древесным спиртом», потому что его когда-то получали сухой перегонкой дерева; систематическое название для этого спирта метанол. Алкалоид морфин назван по его наркотическому действию, но в этом случае тривиальное название является единственным обычно используемым, поскольку систематическое название сложно и громоздко. Тривиальные названия часто дают промышленным продуктам, особенно в фармацевтической промышленности, где продукты продаются под патентованными названиями, причем одно и то же соединение различные фирмы могут выпустить под различными названиями. Часто используются квазисистематические названия, которые не могут адекватно описать структуру соединения без дополнительной информации. Например, инсектицид ДДТ иногда называют дихлордифенилтрихлорэтаном, чего недостаточно, чтобы написать единственную структуру этого соединения, поскольку название ничего не говорит о положении атомов хлора. Полное название для главного активного компонента 2,2-ди(4-хлорфенил)-1,1,1-трихлорэтан.
Основные правила наименования соединений по системе ИЮПАК даны ниже:
1. Находят самую длинную непрерывную цепь углеродных атомов в молекуле. Название соответствующего углеводорода используют как основу названия соединения.
2. Атомам (иным, чем водород) и группам вдоль этой цепи даются наименования, и эти наименования пишут перед названием основного углеводорода.
3. Атомы углерода основной углеводородной цепи нумеруют последовательно, начиная с конца, выбранного так, чтобы атомы углерода, несущие заместители, получили наиболее низкие номера.
4. Положения заместителей указывают локантами числами перед названиями заместителей, обозначающими порядковые номера атомов углерода, к которым они присоединены.
5. Если имеется несколько одинаковых групп, перед их названием ставится приставка «ди», «три», «тетра», «пента», «гекса» и т.д., обозначающая число присутствующих групп.
6. Двойные углерод-углеродные связи указывают суффиксом «ен» («диен», если их две, и т.п.), а тройные суффиксом «ин» («диин» для двух и т.д.); при использовании этих суффиксов окончание «ан» опускают. Положение кратных связей обозначают порядковыми номерами углеродных атомов, подобно тому, как это делается для заместителей.
7. Все название пишется одним словом.
Несколько примеров иллюстрируют эти правила:

Наименование таких сложных радикалов, как CH 3 CHCH 2 Cl в последнем примере, осуществляется по следующим правилам:
1. Углеродный атом со «свободной» связью получает номер 1 ў . Самая длинная углеродная цепь, начиная с этого места, последовательно нумеруется и используется для основного названия (в приведенном примере этан).
2. С заместителями вдоль этой цепи поступают, как описано выше при наименовании соединений.
3. Полное название сложного радикала заключают в скобки, чтобы избежать путаницы с номерами для остальной части молекулы.
Названия по системе ИЮПАК и обычные названия для нескольких часто встречающихся сложных радикалов даны в табл. 2.
Циклические углеводороды называют, прибавляя к названию углеводорода с прямой цепью приставку «цикло». Для указания положения заместителей атомы кольца нумеруют последовательно, начиная с главного заместителя (табл. 3).

Отметим, что в последнем примере углеводород просто называют бензолом (а не 1,3,5-циклогексатриеном), а соответствующий радикал фенилом.
|
Таблица 3. НАЗВАНИЯ НАИБОЛЕЕ ЧАСТО ВСТРЕЧАЮЩИХСЯ ФУНКЦИОНАЛЬНЫХ (ХАРАКТЕРИСТИЧЕСКИХ) ГРУПП ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ (ГРУППЫ ПЕРЕЧИСЛЯЮТСЯ СВЕРХУ ВНИЗ В ПОРЯДКЕ ПОНИЖАЮЩЕГОСЯ СТАРШИНСТВА) |
|||
| Соединения |
Группы |
Названия групп |
|
|
в префиксе |
в суффиксе |
||
| Карбоновые кислоты | –COOH –(C)OOH a |
карбокси-
– |
-карбоновая
кислота
-овая кислота |
| Сульфоновые кислоты | –SO 3 H | сульфо- | -сульфоновая
кислота
(-сульфокислота) |
| Амиды | –CONH 2 –(C)ONH 2 a |
карбамоил-
– |
-карбоксамид
-амид |
| Нитрилы | –Cє
N –(C)є N a |
циано-
– |
-карбонитрил
-нитрил |
| Альдегиды | –CH=O –(C)H=O a |
формил-
оксо- |
-карбальдегид
-аль |
| Кетоны | –(C)=O | оксо- (кето) | -он |
| Спирты, фенолы | –OH | гидрокси- | -ол |
| Тиолы | –SH | меркапто- | -тиол |
| Амины | –NH 2 | амино- | -амин |
| Простые эфиры б | –OAlk | алкокси- | – |
| Галогенопроизводные б | F, Cl, Br, I | фтор-, хлор-, бром-, иод- | – |
| Нитрозосоединения б | –NO | нитрозо- | – |
| Нитросоединения б | –NO 2 | нитро- | – |
| Диазосоединения б | –N 2 | диазо- | – |
| Азиды б | –N 3 | азидо- | – |
|
А
Атом С, взятый в
скобки, считается частью главной углеродной цепи, а не функциональной
группы (CH 3 COOH
– этановая, метанкарбоновая, уксусная кислота).
|
|||
Более сложным циклическим соединениям обычно дают тривиальные названия и системы нумерации. К соединениям этого типа относятся полициклические ароматические углеводороды (в которых бензольные кольца соединены двумя общими атомами) и гетероциклические соединения (у которых в состав колец входят гетероатомы). Важнейшие циклические системы и их нумерация приведены в табл. 4. Отметим, что в гетероциклах нумерация начинается с гетероатома и производится так, чтобы другие гетероатомы получили наименьшие номера. Наименование заместителей в этих кольцах следует основным правилам ИЮПАК, приведенным выше.

Наиболее широко для построения названий органических соединений правила ИЮПАК рекомендуют использовать заместительную номенклатуру. Общая схема таких названий: 1) префиксы боковые цепи, затем младшие функции (см . табл. 3) в алфавитном порядке; 2) корень главная цепь или цикл; 3) суффиксы кратные связи, главная функция. Например

Геометрическую изомерию обозначают приставками цис - и транс - (см. выше ).
Оптическую изомерию обозначают символами D-, L- или мезо - перед названием соединения, чтобы указать ряд, к которому оно принадлежит. Другие системы используются реже. Направление вращения плоскополяризованного света часто указывают знаком (+) для правовращающих и знаком () для левовращающих изомеров.
Для кислот, кроме их систематических наименований, в научной литературе широко используются тривиальные названия. Некоторые важные органические кислоты перечислены ниже (табл. 5 и 6).
Лекция № 1
СОЕДИНЕНИЙ
- Структурная изомерия.
Лекция № 1
КЛАССИФИКАЦИЯ И НОМЕНКЛАТУРА ОРГАНИЧЕСКИХ
СОЕДИНЕНИЙ
- Классификация органических соединений.
- Номенклатура органических соединений.
- Структурная изомерия.
1. Классификация органических соединений.
Органические соединения классифицируют по двум основным признакам: строению
углеродного скелета и функциональным группам.
По строению углеродного скелета различают ациклические, карбоциклические и
гетероциклические соединения.
Ациклические соединения – содержат открытую цепь атомов углерода.
Карбоциклические соединения
– содержат замкнутую цепь углеродных
атомов и подразделяются на алициклические и ароматические. К алициклическим
относятся все карбоциклические соединения, кроме
ароматических. Ароматические
соединения содержат циклогексатриеновый
фрагмент (бензольное ядро).
Гетероциклические соединения
—
содержат циклы, включающие наряду с атомами углерода один
или несколько гетероатомов.
По природе функциональных групп органические
соединения делят на классы
.
Таблица 1. Основные классы органических
соединений.
| Функциональная группа |
Класс соединений |
Общая формула |
| Отсутствует |
Углеводороды |
R-H |
| Галоген F, -Cl, -Br, -I (–Hal) |
Галогенпроизводные |
R-Hal |
| Гидроксильная ОН
|
Спирты и фенолы |
R-OH |
| Алкоксильная |
Простые эфиры |
R-OR |
| Амино NH 2 , >NH, >N- |
Амины |
RNH 2 , R 2 NH, R 3 N |
| Нитро |
Нитросоединения |
RNO 2 |
| Карбонильная |
Альдегиды и кетоны |
|
| Карбоксильная |
Карбоновые кислоты |
|
| Алкоксикарбонильная |
Сложные эфиры |
|
| Карбоксамидная |
Амиды карбоновых кислот
|
|
| Тиольная |
Тиолы |
R-SH |
| Сульфо |
Сульфокислоты |
R-SO 3 H |
2. Номенклатура органических
соединений.
В настоящее время в органической химии общепринятой является систематическая номенклатура,
разработанная
Международным союзом чистой и прикладной химии
(IUPAC
). Наряду с ней сохранились и
используются тривиальная
и рациональная
номенклатуры.
Тривиальная номенклатура
состоит
из исторически сложившихся названий, которые не отражают состава и строения
вещества. Они являются случайными и отражают природный источник вещества
(молочная кислота, мочевина, кофеин), характерные свойства (глицерин, гремучая
кислота), способ получения (пировиноградная кислота, серный эфир), имя
первооткрывателя (кетон Михлера, углеводород Чичибабина), область применения
(аскорбиновая кислота). Преимуществом тривиальных названий является их
лаконичность, поэтому употребление некоторых из них разрешено правилами
IUPAC.
Систематическая номенклатура
является научной и отражает состав, химическое и пространственное строение
соединения. Название соединения выражается при помощи сложного слова, составные
части которого отражают определенные элементы строения молекулы вещества. В
основе правил номенклатуры IUPAC лежат принципы заместительной
номенклатуры
, согласно которой молекулы соединений рассматриваются как
производные углеводородов, в которых атомы водорода замещены на другие атомы или
группы атомов. При построении названия в молекуле соединения выделяют следующие
структурные элементы.
Родоначальная структура
– главная цепь
углеродная цепь или циклическая структура в карбо- и гетероциклах.
Углеводородный радикал
– остаток
формульного обозначения углеводорода со свободными валентностями (см. таблицу
2).
Характеристическая группа
–
функциональная группа, связанная с родоначальной структурой или входящая в ее
состав (см. таблицу 3).
При составлении названия последовательно
выполняют следующие правила.
- Определяют старшую характеристическую
группу и указывают ее обозначение в суффиксе (см. таблицу 3). - Определяют родоначальную структуру по
следующим критериям в порядке падения старшинства: а) содержит старшую
характеристическую группу; б) содержит максимальное число характеристических
групп; в) содержит максимальное число кратных связей; г) имеет максимальную
длину. Родоначальную структуру обозначают в корне названия в соответствии с
длиной цепи или размером цикла: С 1 – “мет”, С 2 – “эт”, С 3 – “проп”, С 4 – “бут”, С 5 и далее – корни греческих числительных. - Определяют степень насыщенности и отражают
ее в суффиксе: “ан” – нет кратных связей, “ен” – двойная связь, “ин” –
тройная связь. - Устанавливают остальные заместители
(углеводородные радикалы и младшие характеристические группы) и перечисляют
их названия в префиксе в алфавитном порядке. - Устанавливают умножающие префиксы – “ди”,
“три”, “тетра”, указывающие число одинаковых структурных элементов (при
перечислении заместителей в алфавитном порядке не учитываются ). - Проводят нумерацию родоначальной структуры
так, чтобы старшая характеристическая группа имела наименьший порядковый
номер. Локанты (цифры) ставят перед названием родоначальной структуры, перед
префиксами и перед суффиксами.
.gif)
Таблица 2. Названия алканов и алкильных
радикалов, принятые систематической номенклатурой IUPAC.
| Алкан |
Название |
Алкильный радикал |
Название |
| CH 4 |
Метан |
СН 3 — |
Метил |
| CH 3 CH 3 |
Этан |
CH 3 CH 2 — |
Этил |
| CH 3 CH 2 CH 3 |
Пропан |
CH 3 CH 2 CH 2 — |
Пропил |
| |
Изопропил |
||
| CH 3 CH 2 СН 2 CH 3 |
н -Бутан |
CH 3 CH 2 СН 2 CH 2 — |
н- Бутил |
| |
втор- Бутил |
||
.gif) |
Изобутан |
 |
Изобутил |
| |
трет- Бутил |
||
| CH 3 CH 2 СН 2 CH 2 СН 3 |
н -Пентан |
CH 3 CH 2 СН 2 CH 2 СН 2 — |
н -Пентил |
.gif) |
Изопентан
|
.gif) |
Изопентил
|
| |
Неопентан
|
|
Неопентил
|
Таблица 3. Названия характеристических
групп
(перечислены в порядке убывания старшинства).
| Группа |
Название |
|
| в префиксе |
в суффиксе |
|
| -(C)OOH * |
— |
овая кислота |
| -COOH |
карбокси |
карбоновая кислота |
| -SO 3 H |
сульфо |
сульфоновая кислота |
| -(C)HO |
оксо |
аль |
| -CHO |
формил |
карбальдегид |
| >(C)=O |
оксо- |
он |
| -ОН |
гидрокси |
ол |
| -SH |
меркапто |
тиол |
| -NH 2 |
амино |
амин |
| -OR ** |
алкокси, арокси |
— |
| -F, -Cl, -Br, -I |
фтор, хлор, бром, иод |
— |
| -NO 2 |
нитро |
— |
* Атом углерода,
заключенный в скобки, входит в состав родоначальной структуры.
** Алкокси-группы и все
следующие за ними перечисляются в префиксе по алфавиту и не имеют порядка
старшинства.
Рациональная (радикально-функциональная)
номенклатура
используется для названий простых моно- и
бифункциональных соединений и некоторых классов природных соединений. Основу
названия составляет название данного класса соединений или одного из членов
гомологического ряда с указанием заместителей. В качестве локантов, как правило,
используются греческие буквы.
.gif)
3. Структурная изомерия.
Изомеры
– это вещества, имеющие одинаковый состав и молекулярную
массу, но разные физические и химические свойства. Различия в свойствах изомеров
обусловлены различиями в их химическом или пространственном строении.
Под химическим строением
понимают природу и последовательность связей
между атомами в молекуле. Изомеры, молекулы которых отличаются по химическому
строению, называют структурными изомерами
.
Структурные изомеры могут отличаться:
- по строению углеродного скелета
.gif)
- по положению кратных связей и
функциональных групп
.gif)
- по типу функциональных групп
.gif)
В ходе урока вы сможете изучить тему «Основные принципы номенклатуры органических соединений». Узнаете названия веществ по номенклатуре IUPAC, которой придерживаются во всем мире, рассмотрите алгоритм выбора основной цепи, порядок составления названия органических соединений. Научитесь составлять названия органических соединений по структурной формуле.
Тема: Введение в органическую химию
Урок: Основные принципы номенклатуры органических соединений
Некоторые названия органических веществ, например, спирт и эфир, пришли к нам еще от алхимиков, очень многие вещества получили свои имена в девятнадцатом веке. Одни названия прямо указывают, из чего было впервые выделено данное вещество: винный спирт, гераниол, яблочная, щавелевая, муравьиная кислоты и т.д. Другие - отражают способ получения вещества: серный эфир, имя открывшего их ученого и т.п.
В настоящее время общепринятой считается номенклатура, разработанная союзом ИЮПАК, хотя до сих пор широко применяются как тривиальные названия (уксусная кислота, мочевина), так и названия, составленные по принципам устаревших номенклатур (изооктан, тетраметилэтилен и т.п.)
· Номенклатура ИЮПАК составлена по заместительному принципу. Считается, что структурная формула состоит из основной цепи - атомов углерода, соединенных между собой в неразветвленную цепочку - и присоединенных к ним заместителей. Заместитель - это любой атом или группа атомов, которые замещают атом водорода в неразветвленной структуре основой цепи.
· Функциональные группы, которые непосредственно связаны с основной цепью или входят в ее состав, в номенклатуре ИЮПАК называют характеристическими группами .
· Название в номенклатуре ИЮПАК состоит из корня, который обозначает длину основной цепи, а также приставок и суффиксов, отражающих наличие и расположение заместителей, кратных связей и функциональных групп.
· Название может содержать все блоки, а может - только два: корень и суффикс кратности связей.
· Корень названия вещества происходит из названий неразветвленных алканов с аналогичной длиной цепи.
Рис. 1. Принципы названий по номенклатуре ИЮПАК
Чтобы составить название вещества, необходимо знать названия неразветвленных алканов. Табл. 1.

Первые четыре названия: метан, этан, пропан и бутан возникли исторически, а остальные происходят от греческих корней, обозначающих число атомов углерода в молекуле.
Все названия неразветвленных алканов состоят из корня и суффикса кратности связи -ан . Этот суффикс обозначает то, что вещество предельно - не содержит двойных и тройных связей.
Двойную связь обозначает суффикс -ен , тройную - -ин .
Неразветвленную цепь можно выбрать разными способами. Для того, чтобы название было однозначным, в номенклатуре существует алгоритм выбора основной цепи.
1. В основную цепь входит «старшая» характеристическая группа.
2. В основную цепь максимально включены характеристические группы и кратные связи.
3. Основная цепь максимально длинная из всех возможных.
4. Основная цепь - самая разветвленная.
Например, в основную цепь необходимо включить кратные связи (правила 2), даже, если она при этом не будет самой длинной (правило 3).
В таблице 2 приведены примеры названий характеристических групп. Стрелочка справа показывает увеличение старшинства: в данной таблице, чем выше группа, тем она «старше». Название старшей характеристической группы определяет суффикс названия вещества. Остальные характеристические группы при этом обозначаются приставками, наравне с прочими заместителями.

Таб. 2. Названия характеристических групп
1. В структурной формуле выбирают основную цепь, используя алгоритм выбора основной цепи.
2. Основную цепь нумеруют так, чтобы старшая характеристическая группа получила наименьший номер. Если такая группа отсутствует, наименьший номер получает кратная связь, причем, принято, что двойная связь старше тройной. В случае отсутствия кратных связей нумерацию проводят так, чтобы заместители получили наименьшие номера.
3. Перечисляют заместители с их номерами в алфавитном порядке, затем записывают корень названия, отвечающий числу атомов углерода в основной цепи, добавляют суффикс кратных связей и суффикс старшей характеристической группы.
4. Если в молекуле присутствует несколько одинаковых заместителей или кратных связей, то употребляют приставку, обозначающую их число (ди-, три-, тетра-, пента-, гекса- и т.д.). Числа в названиях отделяют дефисами, между числами ставят запятые.
В ходе урока вы смогли изучить тему «Основные принципы номенклатуры органических соединений». Вы узнали названия веществ по номенклатуре IUPAC, которой придерживаются во всем мире. Рассмотрели алгоритм выбора основной цепи, порядок составления названия органических соединений. Научились составлять названия органических соединений по структурной формуле.
Список литературы
1. Рудзитис Г.Е. Химия. Основы общей химии. 10 класс: учебник для общеобразовательных учреждений: базовый уровень / Г. Е. Рудзитис, Ф.Г. Фельдман. - 14-е издание. - М.: Просвещение, 2012.
2. Химия. 10 класс. Профильный уровень: учеб. для общеобразоват. учреждений/ В.В. Еремин, Н.Е. Кузьменко, В.В. Лунин и др. - М.: Дрофа, 2008. - 463 с.
3. Химия. 11 класс. Профильный уровень: учеб. для общеобразоват. учреждений/ В.В. Еремин, Н.Е. Кузьменко, В.В. Лунин и др. - М.: Дрофа, 2010. - 462 с.
4. Хомченко Г.П., Хомченко И.Г. Сборник задач по химии для поступающих в вузы. - 4-е изд. - М.: РИА «Новая волна»: Издатель Умеренков, 2012. - 278 с.
Домашнее задание
1. №№ 8, 9 (с. 22) Рудзитис Г.Е., Фельдман Ф.Г. Химия: Органическая химия. 10 класс: учебник для общеобразовательных учреждений: базовый уровень/ Г. Е. Рудзитис, Ф.Г. Фельдман. - 14-е издание. - М.: Просвещение, 2012.
2. Назовите по международной номенклатуре трехатомный спирт глицерин.
3. Напишите структурную формулу 2,5-диметил,3-этилоктана. К какому гомологическому ряду относится это вещество?
Самая простая классификация заключается в том. что все известные вещества делят на неорганические и органические . К органическим веществам относят углеводороды и их производные. Все остальные вещества - неорганические.

Неорганические вещества по составу делят на простые и сложные .

Простые вещества состоят из атомов одного химического элемента и подразделяются на металлы, неметаллы, благородные газы. Сложные вещества состоят из атомов разных элементов, химически связанных друг с другом.
Сложные неорганические вещества по составу и свойствам распределяют по следующим важнейшим классам: оксиды, основания, кислоты, амфотерные гидроксиды, соли.
- Оксиды - это сложные вещества, состоящие из двух химических элементов, один из которых - кислород со степенью окисления (-2). Общая формула оксидов: Э m О n , где m - число атомов элемента Э, а n - число атомов кислорода. Оксиды, в свою очередь, классифицируют на солеобразующие и несолеобрадующие. Солеобразующие делятся на основные, амфотерные, кислотные, которым соответствуют основания, амфотерные гидроксиды, кислоты соответственно.
- Основные оксиды
- это оксиды металлов в степенях окисления +1 и +2. К ним относятся:
- оксиды металлов главной подгруппы первой группы (щелочные металлы ) Li - Fr
- оксиды металлов главной подгруппы второй группы (Mg и щелочноземельные металлы ) Mg - Ra
- оксиды переходных металлов в низших степенях окисления
- Кислотные оксиды -образуют неметаллы со С.О. более +2 и металлы со С.О. от +5 до +7 (SO 2 , SeO 2 , Р 2 O 5 , As 2 O 3 , СO 2 , SiO 2 , CrO 3 и Mn 2 O 7). Исключение: у оксидов NO 2 и ClO 2 нет соответствующих кислотных гидроксидов, но их считают кислотными.
- Амфотерные оксиды -образованы амфотерными металлами со С.О. +2, +3,+4 (BeO, Cr 2 O 3 , ZnO, Al 2 O 3 , GeO 2 , SnO 2 и РЬО).
- Несолеобразующие оксиды - оксиды неметаллов со С.О.+1, +2 (СО, NO, N 2 O, SiO).
- Основания - это сложные вещества, состоящие из атомов металла и одной или нескольких гидроксогрупп (-ОН). Общая формула оснований: М(ОН) у, где у - число гидроксогрупп, равное степени окислении металла М (как правило, +1 и +2). Основания делятся на растворимые (щелочи) и нерастворимые.
- Кислоты -(кислотные гидроксиды)- это сложные вещества, состоящие из атомов водорода, способных замещаться на атомы металла, и кислотных остатков. Общая формула кислот: Н х Ас, где Ас - кислотный остаток (от английского «acid» - кислота), х - число атомов водорода, равное заряду иона кислотного остатка.
- Амфотерные гидроксиды - это сложные вещества, которые проявляют и свойства кислот, и свойства оснований. Поэтому формулы амфотерных гидроксидов можно записывать и в форме кислот, и в форме оснований.
- Соли - это сложные вещества, состоящие из катионов металла и анионов кислотных остатков. Такое определение относится к средним солям.
- Средние соли - это продукты полного замещения атомов водорода в молекуле кислоты атомами металла или полного замещения гидроксогрупп в молекуле основания кислотными остатками.
- Кислые соли - атомы водорода в кислоте замещены атомами металла частично. Они получаются при нейтрализации основания избытком кислоты. Чтобы правильно назвать кислую соль, необходимо к названию нормальной соли прибавить приставку гидро- или дигидро- в зависимости от числа атомов водорода, входящих в состав кислой соли.Например, KHCO 3 – гидрокарбонат калия, КH 2 PO 4 – дигидроортофосфат калия. Нужно помнить, что кислые соли могут образовывать только двух и более основные кислоты.
- Осно́вные соли - гидроксогруппы основания (OH −) частично замещены кислотными остатками. Чтобы назвать основную соль, необходимо к названию нормальной соли прибавить приставку гидроксо- или дигидроксо- в зависимости от числа ОН – групп, входящих в состав соли.Например, (CuOH) 2 CO 3 – гидроксокарбонат меди (II).Нужно помнить, что основные соли способны образовывать лишь основания, содержащие в своём составе две и более гидроксогрупп.
- Двойные соли - в их составе присутствует два различных катиона, получаются кристаллизацией из смешанного раствора солей с разными катионами, но одинаковыми анионами. Например, KAl(SO 4) 2 , KNaSO 4.
- Смешанные соли - в их составе присутствует два различных аниона. Например, Ca(OCl)Cl.
- Гидратные соли (кристаллогидраты ) - в их состав входят молекулы кристаллизационной воды. Пример: Na 2 SO 4 ·10H 2 O.

Классификация органических веществ
Соединения, состоящие только из атомов водорода и углерода, называют углеводородами . Прежде чем начать данный раздел, запомни, для упрощения записи, химики не расписывают в цепочках углероды и водороды, однако не забывай что углерод образует четыре связи, и если на рисунке углерод связан двумя связями, то еще двумя он связан с водородами, хоть последнее и не указано:

В зависимости от строения углеродной цепи органические соединения разделяют на соединения с открытой цепью - ациклические (алифатические) и циклические - с замкнутой цепью атомов.
Циклические делятся на две группы: карбоциклические соединения и гетероциклические .
Карбоциклическне соединения , в свою очередь, включают два ряда соединений: алициклические и ароматические .
Ароматические соединения в основе строения молекул имеют плоские углеродсодержащие циклы с особой замкнутой системой π-электронов. образующих общую π-систему (единое π-электронное облако).

Как ациклические (алифатические), так и циклические углеводороды могут содержать кратные (двойные или тройные) связи. Такие углеводороды называют непредельными (ненасыщенными), в отличие от предельных (насыщенных), содержащих только одинарные связи.
Пи-связь (π-связь) - ковалентная связь, образующаяся перекрыванием p-атомных орбиталей. В отличие от сигма-связи, осуществляемой перекрыванием s-атомных орбиталей вдоль линии соединения атомов, пи-связи возникают при перекрывании p-атомных орбиталей по обе стороны от линии соединения атомов.
В случае образования ароматической системы, например, бензола C6H6, каждый из шести атомов углерода находится в состоянии sp2 - гибридизации и образует три сигма-связи с валентными углами 120 °. Четвёртый p-электрон каждого атома углерода ориентируется перпендикулярно к плоскости бензольного кольца. В целом возникает единая связь, распространяющаяся на все атомы углерода бензольного кольца. Образуются две области пи-связей большой электронной плотности по обе стороны от плоскости сигма-связей. При такой связи все атомы углерода в молекуле бензола становятся равноценными и, следовательно, подобная система более устойчива, чем система с тремя локализованными двойными связями.

Предельные алифатические углеводороды называют алканами, они имеют общую формулу С n Н 2n + 2 , где n - число атомов углерода. Старое их название часто употребляется и в настоящее время - парафины:
Непредельные алифатические углеводороды с одной тройной связью называют алкинами. Их общая формула С n Н 2n — 2
Предельные алициклические углеводороды - циклоалканы, их общая формула С n Н 2n:

Мы рассмотрели классификацию углеводородов. Но если в этих молекулах один или большее число атомов водорода заменить на другие атомы или группы атомов (галогены, гидроксильные группы, аминогруппы и др.), образуются производные углеводородов: галогенопроизводные, кислородсодержащие, азотсодержащие и другие органические соединения.

Атомы или группы атомов, которые определяют самые характерные свойства данного класса веществ, называются функциональными группами.
Углеводороды в их производные с одной и той же функциональной группой образуют гомологические ряды.
Гомологическим рядом называют ряд соединений, принадлежащих к одному классу (гомологов), по отличающихся друг от друга по составу на целое число групп -СН 2 - (гомологическую разность), имеющих сходное строение и, следовательно, сходные химические свойства.
Сходство химических свойств гомологов значительно упрощает изучение органических соединений.
Замещенные углеводороды
- Галогенопроизводные углеводородов можно рассматривать как продукты замещения в углеводородах одного или нескольких атомов водорода атомами галогенов. В соответствии с этим могут существовать предельные и непредельные моно-, ли-, три- (в общем случае поли-) галогенопроизводные.Общая формула галогенопроизводных предельных углеводородов R-Г.К кислородсодержащим органическим веществам относят спирты, фенолы, альдегиды, кетоны, карбоновые кислоты, простые и сложные эфиры.
- Спирты - производные углеводородов, в которых один или несколько атомов водорода замещены на гидроксильные группы.Спирты называют одноатомными, если они имеют одну гидроксильную группу, и предельными, если они - производные алканов.Общая формула предельных одноатомных спиртов: R-ОН.
- Фенолы - производные ароматических углеводородов (ряда бензола), в котором один или несколько атомов водорода в бензольном кольце замещены на гидроксильные группы.
- Альдегиды и кетоны - производные углеводородов, содержащие карбонильную группу атомов (карбонил).В молекулах альдегидов одна связь карбонила идет на соединение с атомом водорода, другая - с углеводородным радикалом.В случае кетонов карбонильная группа связана с двумя (в общем случае разными) радикалами.
- Простые эфиры представляют собой органические вещества, содержащие два углеводородных радикала, соединенные атомом кислорода: R=О-R или R-О-R 2 .Радикалы могут быть одинаковыми или разными. Состав простых эфиров выражается формулой С n Н 2n +2O.
- Сложные эфиры - соединения, образованные замещением атома водорода карбоксильной группы в карбоновых кислотах на углеводородный радикал.
- Нитросоединения - производные углеводородов, в которых один или несколько атомов водорода замещены на нитрогруппу -NO 2 .
- Амины - соединения, которые рассматривают как производные аммиака, в котором атомы водорода замещены на углеводородные радикалы.В зависимости от природы радикала амины могут быть алифатическими. В зависимости от числа замещенных на радикалы атомов водорода различают первичные амины, вторичные, третичные. В частном случае у вторичных, а также третичных аминов радикалы могут быть и одинаковыми. Первичные амины можно также рассматривать как производные углеводородов (алканов), в которых один атом водорода замещен на аминогруппу. Аминокислоты содержат две функциональные группы, соединенные с углеводородным радикалом, - аминогруппу -NH 2 и карбоксил -СOОН.
Известны и другие важные органические соединения, которые имеют несколько разных или одинаковых функциональных групп, длинные линейные цепи, связанные с бензольными кольцами. В таких случаях строгое определение принадлежности вещества к какому-то определенному классу невозможно. Эти соединения часто выделяют в специфические группы веществ: углеводы, белки, нуклеиновые кислоты, антибиотики, алкалоиды и др. В настоящее время известно также много соединений, которые можно отнести и к органическим, и к неорганическим. Их называют элементоорганическими соединениями. Некоторые из них можно рассматривать как производные углеводородов.
Номенклатура
Для названия органических соединений используют 2 номенклатуры – рациональную и систематическую (ИЮПАК) и тривиальные названия .

Составление названий по номенклатуре ИЮПАК:
1) Основу названия соединения составляет корень слова, обозначающий предельный углеводород с тем же числом атомов, что и главная цепь.
2) К корню добавляют суффикс, характеризующий степень насыщенности:
Ан (предельный, нет кратных связей);
Ен (при наличии двойной связи);
Ин (при наличии тройной связи).

Если кратных связей несколько, то в суффиксе указывается число таких связей (-диен, -триен и т.д.), а после суффикса обязательно указывается цифрами положение кратной связи, например:
СН 3 –СН 2 –СН=СН 2 СН 3 –СН=СН–СН 3
бутен-1 бутен-2
СН 2 =СН–СН=СН 2
Такие группы как нитро-, галогены, углеводородные радикалы, не входящие в главную цепь выносятся в приставку. При этом они перечисляются по алфавиту. Положение заместителя указывается цифрой перед приставкой.
Порядок составления названия следующий:
1. Найти самую длинную цепь атомов С.
2. Последовательно пронумеровать атомы углерода главной цепи, начиная с ближайшего к разветвлению конца.
3. Название алкана складывается из названий боковых радикалов, перечисленных в алфавитном порядке с указанием положения в главной цепи, и названия главной цепи.
 Порядок составления названия
Порядок составления названия
Химический язык, в состав которого в качестве одной из наиболее специфических частей входит химическая символика (включающая и химические формулы), является важным активным средством познания химии и требует поэтому четкого и осознанного применения.
Химические формулы — это условные изображения состава и строения химически индивидуальных веществ посредством химических символов, индексов и других знаков. При изучении состава, химического, электронного и пространственного строения веществ, их физических и химических свойств, изомерии и других явлений применяют химические формулы разных видов.
Особенно много видов формул (простейшие, молекулярные, структурные, проекционные, конформационные и др.) применяют при изучении веществ молекулярного строения — большинства органических веществ и сравнительно небольшой части неорганических веществ при обычных условиях. Значительно меньше видов формул (простейшие) применяют при изучении немолекулярных соединений, строение которых более наглядно отражают шаростержневые модели и схемы кристаллических структур или их элементарных ячеек.

Составление полных и кратких структурных формул углеводородов
Пример:
Составить полную и краткую структурные формулы пропана С 3 Н 8 .
Решение:
1. Записать в строчку 3 атома углерода, соединить их связями:
С–С–С
2. Добавить черточки (связи) так, чтобы от каждого атома углерода отходило 4 связи:
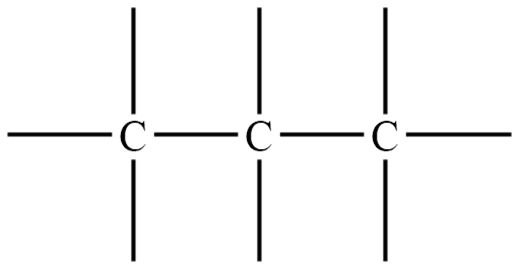

4. Записать краткую структурную формулу:
СН 3 –СН 2 –СН 3
Таблица растворимости
Некоторые названия органических веществ, например, спирт и эфир, пришли к нам еще от алхимиков, очень многие вещества получили свои имена в девятнадцатом веке. Одни названия прямо указывают, из чего было впервые выделено данное вещество: винный спирт, гераниол, яблочная, щавелевая, муравьиная кислоты и т.д. Другие - отражают способ получения вещества: серный эфир, имя открывшего их ученого и т.п.
В настоящее время общепринятой считается номенклатура, разработанная союзом ИЮПАК, хотя до сих пор широко применяются как тривиальные названия (уксусная кислота, мочевина), так и названия, составленные по принципам устаревших номенклатур (изооктан, тетраметилэтилен и т.п.)
· Номенклатура ИЮПАК составлена по заместительному принципу. Считается, что структурная формула состоит из основной цепи - атомов углерода, соединенных между собой в неразветвленную цепочку - и присоединенных к ним заместителей. Заместитель - это любой атом или группа атомов, которые замещают атом водорода в неразветвленной структуре основой цепи.
· Функциональные группы, которые непосредственно связаны с основной цепью или входят в ее состав, в номенклатуре ИЮПАК называют характеристическими группами .
· Название в номенклатуре ИЮПАК состоит из корня, который обозначает длину основной цепи, а также приставок и суффиксов, отражающих наличие и расположение заместителей, кратных связей и функциональных групп.
· Название может содержать все блоки, а может - только два: корень и суффикс кратности связей.
· Корень названия вещества происходит из названий неразветвленных алканов с аналогичной длиной цепи.
Рис. 1. Принципы названий по номенклатуре ИЮПАК
Чтобы составить название вещества, необходимо знать названия неразветвленных алканов. Табл. 1.

Первые четыре названия: метан, этан, пропан и бутан возникли исторически, а остальные происходят от греческих корней, обозначающих число атомов углерода в молекуле.
Все названия неразветвленных алканов состоят из корня и суффикса кратности связи -ан . Этот суффикс обозначает то, что вещество предельно - не содержит двойных и тройных связей.
Двойную связь обозначает суффикс -ен , тройную - -ин .
Неразветвленную цепь можно выбрать разными способами. Для того, чтобы название было однозначным, в номенклатуре существует алгоритм выбора основной цепи.
1. В основную цепь входит «старшая» характеристическая группа.
2. В основную цепь максимально включены характеристические группы и кратные связи.
3. Основная цепь максимально длинная из всех возможных.
4. Основная цепь - самая разветвленная.
Например, в основную цепь необходимо включить кратные связи (правила 2), даже, если она при этом не будет самой длинной (правило 3).
В таблице 2 приведены примеры названий характеристических групп. Стрелочка справа показывает увеличение старшинства: в данной таблице, чем выше группа, тем она «старше». Название старшей характеристической группы определяет суффикс названия вещества. Остальные характеристические группы при этом обозначаются приставками, наравне с прочими заместителями.

Таб. 2. Названия характеристических групп
1. В структурной формуле выбирают основную цепь, используя алгоритм выбора основной цепи.
2. Основную цепь нумеруют так, чтобы старшая характеристическая группа получила наименьший номер. Если такая группа отсутствует, наименьший номер получает кратная связь, причем, принято, что двойная связь старше тройной. В случае отсутствия кратных связей нумерацию проводят так, чтобы заместители получили наименьшие номера.
3. Перечисляют заместители с их номерами в алфавитном порядке, затем записывают корень названия, отвечающий числу атомов углерода в основной цепи, добавляют суффикс кратных связей и суффикс старшей характеристической группы.
4. Если в молекуле присутствует несколько одинаковых заместителей или кратных связей, то употребляют приставку, обозначающую их число (ди-, три-, тетра-, пента-, гекса- и т.д.). Числа в названиях отделяют дефисами, между числами ставят запятые.
В ходе урока вы смогли изучить тему «Основные принципы номенклатуры органических соединений». Вы узнали названия веществ по номенклатуре IUPAC, которой придерживаются во всем мире. Рассмотрели алгоритм выбора основной цепи, порядок составления названия органических соединений. Научились составлять названия органических соединений по структурной формуле.
источник видео - http://www.youtube.com/watch?t=1&v=DsF0Bx7FZKc
http://www.youtube.com/watch?t=11&v=z1UpyJY1U78
http://www.youtube.com/watch?t=110&v=HJnyF4Vfoy8
источник презентации - http://www.openclass.ru/node/222808
http://interneturok.ru/ru/school/chemistry/10-klass = конспект





